Une question à nos experts en électrochimie sur le fonctionnement des batteries !
Comment se fait-il qu’au cœur d’une batterie, électrons et ions ne prennent pas le même chemin ?
Cette question a été récemment posée dans le cadre d’un webinaire réservé à nos installateurs Storelio.
Les batteries sont des équipements qui transforment l’énergie chimique en énergie électrique et vice-versa.
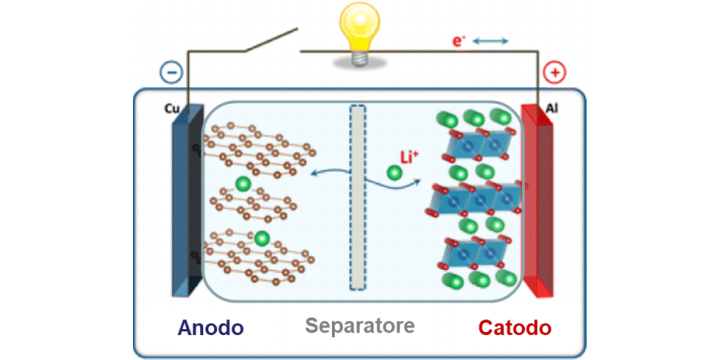
Les batteries sont composées de deux électrodes (bornes + et -) environnées d’un matériau conducteur ionique (électrolyte) et isolées électriquement par un séparateur. Lorsqu’un équipement est connecté aux bornes de la batterie, une réaction d’oxydation se produit à l’anode qui va libérer des électrons et des ions lithium.
Les électrons chargés négativement sont attirés par la cathode et passent par le circuit électrique en alimentant l’équipement tandis que les ions transitent de l’anode vers la cathode à l’intérieur de la batterie.
Enfin, les électrons et les ions se rejoignent à la cathode où se produit une réaction de réduction.
Pour résumer, à l’intérieur de la batterie, les transferts d’énergie sont uniquement chimiques (ions transitant entre les 2 électrodes), tandis que les électrons (l’électricité) transitent entre les bornes de la batterie au travers de l’équipement alimenté.